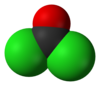
Fozgen
Fozgen (COCl2) je bezbojan gas koji se na temperaturi nižoj od 8.2° C kondenzuje u bezbojnu, uljastu, vrlo isparljivu tečnost. Ovaj bezbojni gas je po zlu poznat zbog njegove upotrebe kao hemijsko oružje tokom Prvog svetskog rata. U niskim koncentracijama, njegov miris podseća na sveže pokošeno seno ili travu. Neki vojnici tokom Prvog svetskog rata su tvrdili da je donekle mirisao poput majskog cvetanja. On je takođe važan industrijski reagens i gradivni blok u sintezi farmaceutskih i drugih organskih jedinjenja. Pored industrijske primene, male količine se prirodno javljaju usled razlaganja i sagorevanja organo-hlornih jedinjenja.[5] Uprkos tome što mu ime sadrži prefiks „fos-“, ne sadrži fosfor.
| |||
| Nazivi | |||
|---|---|---|---|
| IUPAC nazivs
karbonil dihlorid
Dihlorometanal Karbonil hlorid | |||
| Drugi nazivi
CG; ugljen dihlorid oksid; ugljen oksihlorid; karbonil dihlorid; hloroformil hlorid; dihloroformaldehid; dihlorometanon
| |||
| Identifikacija | |||
3D model (Jmol)
|
|||
| ECHA InfoCard | 100.000.792 | ||
| EC broj | 200-870-3 | ||
| RTECS | SY5600000 | ||
| UN broj | 1076 | ||
| |||
| Svojstva | |||
| CCl2O | |||
| Molarna masa | 98,92 g mol-1[4] | ||
| Agregatno stanje | bezbojan gas | ||
| Gustina | 4,248 g/cm3 (15 °C) 1.432 g/cm3 (0 °C) | ||
| Tačka topljenja | −118 °C (−180 °F; 155 K) | ||
| Tačka ključanja | 83 °C (181 °F; 356 K) | ||
| hidroliza | |||
| Rastvorljivost | u benzenu, toluenu, sirćetnoj kiselini razlaže se u alkoholu i kiselinama | ||
| Struktura | |||
| Oblik molekula (orbitale i hibridizacija) | planaran, trigonalan | ||
| Dipolni moment | 1.17 D | ||
| Opasnosti | |||
EU klasifikacija (DSD)
|
Veoma toksičan (T+) | ||
| R-oznake | R26 R34 | ||
| S-oznake | (S1/2) S9 S26 S36/37/39 S45 | ||
| NFPA 704 | |||
| Tačka paljenja | nezapaljiv | ||
| 0.1 ppm | |||
| Srodna jedinjenja | |||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |||
| Reference infokutije | |||
Struktura i osnovne osobine
urediFozgen je planarni molekul. Dužina C=O veze je 1,18 Å, C---Cl dužina je 1,74 Å i Cl---C---Cl ugao je 111,8°.[6] Ovo je jedano od najjednostavnijih kiselih hlorida, formalno izvedenih iz ugljene kiseline.
Tehnički proizvod je bledožute ili crvenkastožute boje mirisa na trulo seno. Pare su mu 3,48 puta teže od vazduha. Dobro se rastvara u organskim rastvaračima dok se u vodi razlaže na ugljen-dioksid i hlorovodonik.
Dobijanje
urediIndustrijski, fozgen se proizvodi putem provođenja prečišćenih gasova ugljen-monoksida i hlora kroz porozni aktivirani ugljenik, koji služi kao katalizator:[5]
- CO + Cl2 → COCl2 (ΔHrxn = −107.6kJ/mol)
Ova reakcija je egzotermna, tako da se mora hladiti. Tipično, ova reakcija se izvodi na temperaturi od 50 do 150 °C. Iznad 200 °C, fozgen se razlaže u ugljen-monoksid i hlor, Keq (300K) = 0,05. Oko 5000 tona je proizvedeno 1989. godine.
Toksičnost
urediFozgen spada u najtoksičnije gasove koji se sreću u industriji. Toksični efekti se ispoljavaju već pri koncentracijama od 3 do 5 ppm, izraženi su pri koncentraciji od 25 ppm, a koncentracije od 50 do 80 ppm dovode do smrti.
Reference
uredi- ^ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0911910131.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ a b Wolfgang Schneider & Werner Diller (2002). „Phosgene”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a19_411.
- ^ Nakata, M.; Kohata, K.; Fukuyama, T.; Kuchitsu, K. (1980). „Molecular Structure of Phosgene as Studied by Gas Electron Diffraction and Microwave Spectroscopy. The rz Structure and Isotope Effect”. Journal of Molecular Spectroscopy. 83: 105—117. doi:10.1016/0022-2852(80)90314-8.
Literatura
uredi- Wolfgang Schneider & Werner Diller (2002). „Phosgene”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a19_411.