Угљенични циклус
Угљенични циклус је биогеохемијски циклус, у којем се угљеник размењује између биосфере, педосфере, геосфере, хидросфере и атмосфере на Земљи. То је један од најважнијих циклуса на Земљи и омогућаве да угљеник поновно искористе нови организми.
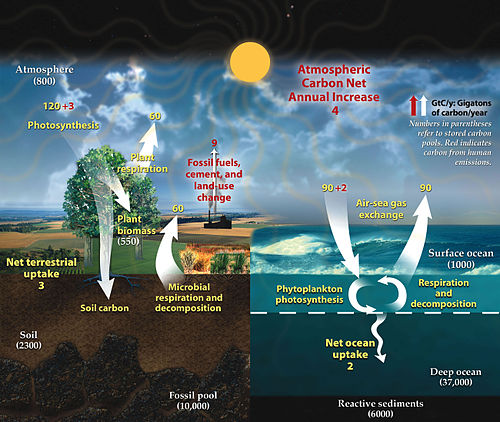
Угљенични циклус су открили Антоан Лавоазје и Џозеф Пристли, а касније је идеју развио Хамфри Дејви.[1]
Главне компоненте
уреди| Резервоар | Количина (гигатона) |
|---|---|
| Атмосфера | 720 |
| Океани (укупно) | 38.400 |
| Укупно неорганки | 37.400 |
| Укупно органски | 1.000 |
| Површински слој | 670 |
| Дубоки слојг | 36.730 |
| Литосфера | |
| Седиментарни карбонати | > 60.000.000 |
| Керогени | 15.000.000 |
| Копнена биосфера (укупно) | 2.000 |
| Жива биомаса | 600 - 1.000 |
| Мртва биомаса | 1.200 |
| Акватична биосфера | 1 - 2 |
| Госилна горива (укупно) | 4.130 |
| Угаљ | 3.510 |
| Нафта | 230 |
| Гас | 140 |
| Друго (тресет) | 250 |
Угљеников циклус обухвата следеће главне спремнике угљеника:
- Земљина атмосфера
- Земљина биосфера, која обично обухвата системе слатке воде и неживе органске материјале, као што је угљеник у тлу.
- Океани, укључујући растворени неоргански угљеник, те све живе и неживе морске организме
- Седименти, укључујући фосилна горива
- Земљина унутрашњост, а то се односи на угљеник који се налази у Земљиној кори и плашту, а испушта се у атмосферу и хидросферу преко вулкана и геотермалних извора
Годишње кретање угљеника или размена између спремника, се јавља због различитих хемијских, геолошких и биолошких процеса. Океан садржи највећи спремник угљеника, али делови у дубоким океанима се не размењују тако брзо с атмосфером.
Прорачун светског угљеника је равнотежа размена (улаза и излаза) угљеника између разних спремника. Тај прорачун указује на то да ли неки спремник служи као извор, или као место таложења угљеника.
Угљеник у Земљиној атмосфери
уредиУ Земљиној атмосфери угљеник првенствено постоји као гас угљен диоксид (CO2). Иако је присутан у само малом уделу (око 0,039%), игра врло важну улогу у одржању живота. Остали гасови који садрже угљеник су метан и хлорофлуороугљеници (CFC или фреони – само због људског утицаја). Стабла, траве и остале зелене биљке, претварају угљен диоксид у угљене хидрате, процесом који се назива фотосинтеза, ослобађајући кисеоник у ваздух. Тај процес је прилично заступљен код нових шума, где стабла још увек расту. Код белогоричних шума је тај процес најјачи у пролеће, кад се ствара лишће. То је добро видљиво на Килинговој кривој мерења концентрације угљен диоксида. Превладава највише на северној хемисфери у пролеће, јер јужна хемисфера нема толико копна у умереном појасу.
- Шуме садрже 86% угљеника изнад тла и 73% угљеника у тлу, на Земљи. [3]
- Површина океана према половима има све више угљеника, јер што је морска вода хладнија, то може да раствори више угљен диоксида из ваздуха, претварајући је у угљену киселину (H2CO3). Значајну улогу игра термохалинска покретна трака, која пребацује гушћу површинку воду у унутрашњост океана.
- У горњим подручјима океана, постоји велика биолошка продуктивност, организми претварају угљеник у ткива или карбонате за тврде заштитне оклопе, као што су шкољке или пужеви. Углавном се угљеник таложи.
- Разградња угљено-силикатних стена. Угљена киселина реагује с разграђеним стенама и ствара бикарбонатне јоне, које користе морски организми за стварање заштитног тврдог слоја. Овај угљеник се не враћа поновно у атмосферу.
- Године 1958. је измерено у опсерваторији Мауна Лоа, на Хавајима, да има 0,032% угљен диоксида, док је 2010. измерено 0,0385% угљен диоксида у атмосфери.[4]
Метан производи већи ефекат стаклене баште по запремини у поређењу са угљен-диоксидом, али постоји у знатно нижим концентрацијама и краткотрајнији је од угљен-диоксида, чинећи угљен-диоксид важнијим гасом стаклене баште.[5]
Угљеник се ослобађа у атмосферу на неколико начина:
- преко дисања, које врше биљке и животиње. То је егзотермна реакција, која ослобађа енергију у облику топлоте, а тиме је обухваћено разлагање молекула угљених хидрата на угљен диоксид и воду.
- преко распадања животиња и биљака. Гљиве и бактерије разлажу угљеникова једињења код мртвих животиња и биљака, претварајући угљеник у угљен диоксид или метан.
- преко изгарања органских материја, које оксидирају угљеник у угљен диоксид. Фосилна горива као што су нафта, угаљ и природни гас, ослобађају угљеник у облику угљен диоксида, који је био милионима година одложен у геосфери. Изгарање биогорива исто ослобађа угљен диоксид, који је био одложен само пар година.
- преко производње цемента. Угљен диоксид се ослобађа када се загрева кречњак (CaCO3), да би се добио креч (CaO), као састојак цемента.
- у деловима океана који су топлији, растворени угљен диоксид се враћа у атмосферу
- вулканске ерупције и рекристализација стена, ослобађају гасове у атмосферу. Вулкански гасови су пре свега водена пара, угљен диоксид и сумпор диоксид.
Угљеник у биосфери
уредиУгљеник је основни састојак живота на Земљи. Око половине суве тежине (без воде) живих организама је угљеник. Он игра важну улогу у изградњи ћелијске опне, у биохемији и исхрани свих живих ћелија. Живи организми садрже око 575 x 1012 кг угљеника,[6] од чега највише имају стабла. Земља има око 1.500 x 1012 кг угљеника, углавном у облику органског угљеника.[7]
- Аутотрофи су организми који стварају своју органску грађу, користећи угљен диоксид из ваздуха или из воде у којој живе. За то користе спољашњу енергију, а то је углавном сунчева енергија, која омогућује фотосинтезу. Врло мали број аутотрофа користи хемијску енергију у процесу хемосинтезе. Најважнији аутотрофи су фитопланктони у морима и океанима, те стабла на копну. Фотосинтеза следи хемијску реакцију: 6CO2 + 6H2O → C6H12O6 + 6O2
- Угљеник се преноси из биосфере хетеротрофијом, а то је храњење на туђим организмима или делу организма. То укључује гљиве или бактерије које користе мртви материјал, процесом врења или распадањем.
- Већина угљеника напушта биосферу преко ћелијског дисања, које ослобађа угљен диоксид, хемијском реакцијом C6H12O6 + 6O2 → 6CO2 + 6H2O. Други облик је ванћелијско дисање, којим се ослобада метан у околину, атмосферу или хидросферу (мочварни гас).
- Изгарање биомаса (шумски пожари, дрво за горење) исто ослобађа знатну количину угљен диоксида у атмосферу.
- Угљеник може кружити кроз биосферу као мртва материја (као тресет), која остаје у геосфери. Егзоскелет или калцијум карбонат из љуштура животиња, може постати кречњак кроз процес седиментације.
- Угљеник кружи и у дубоком океану, где се одређене врсте љускара, које исто стварају тврду заштиту, таложе на дну океана.[8]
Угљеник у хидросфери
уредиОкеани садрже око 36.000 x 1012 кг угљеника, углавном у облику бикарбонатних јона. Екстремне олује, као што су урагани и тајфуни, таложе велике количине угљеника, будући да испирају велике количине седимената. Једна студија у Тајвану је утврдила да је један тајфун испрао више угљеника у океан, него кише које падају целе године. Ти бикарбонатни јони су врло важни за успостављање пХ вредности у океанима.
Угљеник се стално размењује између океана и атмосфере. У подручју узлазних струја, угљеник се ослобађа у атмосферу. Супротно, падалине преносе угљен диоксид у океане. Када се угљен диоксид раствори у океану, томе следи читав низ хемијских реакција, које су у равнотежи у одређеном делу:
Растварање:
- CO2(atmosferski) ⇌ CO2(otopljen)
Претварање у угљеничу киселину:
- CO2(rastvoren) + H2O ⇌ H2CO3
Прва јонизација:
- H2CO3 ⇌ H+ + HCO3− (бикарбонатни јон)
Друга јонизација:
- HCO3− ⇌ H+ + CO3−− (карбонатни јон)
Равнотежа тих процеса се испитује мерењима, која су показала да је количина раствореног угљеника у океанима око 10% количине угљеника у атмосфери. Ако се количина угљен диоксида повећа за 10% у атмосфери, количина раствореног угљеника у океанима се повећа за 1%.[9]
У океанима, растворени карбонати углавном реагују с калцијумом, стварајући нерастворни калцијум карбонат или кречњак (CaCO3), углавном као заштитне кућице за микроскопске организме. Након што ти организми угину, кречњак се таложи на дну, што преставља највећи спремник у угљениковом циклусу.
Референце
уреди- ^ Холмес, Рицхард . "Тхе Аге Оф Wондер", Пантхеон Боокс. 2008. ISBN 978-0-375-42222-5.
- ^ Falkowski, P.; Scholes, R. J.; Boyle, E.; Canadell, J.; Canfield, D.; Elser, J.; Gruber, N.; Hibbard, K.; Högberg, P.; Linder, S.; MacKenzie, F. T.; Moore b, 3.; Pedersen, T.; Rosenthal, Y.; Seitzinger, S.; Smetacek, V.; Steffen, W. (2000). „The Global Carbon Cycle: A Test of Our Knowledge of Earth as a System”. Science. 290 (5490): 291—296. Bibcode:2000Sci...290..291F. PMID 11030643. doi:10.1126/science.290.5490.291.
- ^ Sedjo, Roger.1993. "The Carbon Cycle and Global Forest Ecosystem, Water, Air, and Soil Pollution", Oregon Wild Report on Forests, Carbon, and Global Warming Архивирано на сајту Wayback Machine (28. јун 2010))
- ^ [1] Трендс ин Царбон Диоxиде — НОАА Еартх Сyстем Ресеарцх Лабораторy
- ^ Форстер, П.; Рамаwамy, V.; Артаxо, П.; Бернтсен, Т.; Беттс, Р.; Фахеy, D.W.; Хаywоод, Ј.; Леан, Ј.; Лоwе, D.C.; Мyхре, Г.; Нганга, Ј.; Принн, Р.; Рага, Г.; Сцхулз, M.; Ван Дорланд, Р. (2007). „Цхангес ин атмоспхериц цонституентс анд ин радиативе форцинг”. Цлимате Цханге 2007: тхе Пхyсицал Басис. Цонтрибутион оф Wоркинг Гроуп I то тхе Фоуртх Ассессмент Репорт оф тхе Интерговернментал Панел он Цлимате Цханге.
- ^ Сторинг Царбон ин Соил: Wхy анд Хоw?
- ^ "Сеqуестратион оф атмоспхериц ЦО2 ин глобал царбон поолс" Лал Раттан, јоурнал = Енергy анд Енвиронментал Сциенце, 2008.
- ^ ""Синкерс" провиде миссинг пиеце ин дееп-сеа пуззле", публисхер=Монтереy Баy Аqуариум Ресеарцх Институте МБАРИ), 2005. [2]
- ^ Миллеро Франк: "Цхемицал Оцеанограпхy", публисхер=ЦРЦ Пресс, 2005.
Литература
уреди- Тхе Царбон Цyцле, упдатед пример бy НАСА Еартх Обсерваторy, 2011
- Аппензеллер, Тим (2004). „Тхе цасе оф тхе миссинг царбон”. Натионал Геограпхиц Магазине. – артицле абоут тхе миссинг царбон синк
- Болин, Берт; Дегенс, Е. Т.; Кемпе, С.; Кетнер, П. (1979). Тхе глобал царбон цyцле. Цхицхестер ; Неw Yорк: Публисхед он бехалф оф тхе Сциентифиц Цоммиттее он Проблемс оф тхе Енвиронмент (СЦОПЕ) оф тхе Интернатионал Цоунцил оф Сциентифиц Унионс (ИЦСУ) бy Wилеy. ИСБН 978-0-471-99710-8. Приступљено 2008-07-08.
- Хоугхтон, Р. А. (2005). „Тхе цонтемпорарy царбон цyцле”. Ур.: Wиллиам Х Сцхлесингер. Биогеоцхемистрy. Амстердам: Елсевиер Сциенце. стр. 473–513. ИСБН 978-0-08-044642-4.
- Јанзен, Х. Х. (2004). „Царбон цyцлинг ин еартх сyстемс—а соил сциенце перспецтиве”. Агрицултуре, Ецосyстемс & Енвиронмент. 104 (3): 399—417. дои:10.1016/ј.агее.2004.01.040.
- Миллеро, Франк Ј. (2005). Цхемицал Оцеанограпхy (3 изд.). ЦРЦ Пресс. ИСБН 978-0-8493-2280-8.
- Сундqуист, Ериц; Броецкер, Wаллаце С., ур. (1985). Тхе Царбон Цyцле анд Атмоспхериц ЦО2: Натурал вариатионс Арцхеан то Пресент. Геопхyсицал Монограпхс Сериес. Америцан Геопхyсицал Унион.
Спољашње везе
уреди- Царбон Цyцле Сциенце Програм – ан интерагенцy партнерсхип.
- НОАА'с Царбон Цyцле Греенхоусе Гасес Гроуп
- Глобал Царбон Пројецт – инитиативе оф тхе Еартх Сyстем Сциенце Партнерсхип
- УНЕП – Тхе пресент царбон цyцле – Цлимате Цханге царбон левелс анд флоwс Архивирано на сајту Wayback Machine (15. септембар 2008)
- НАСА'с Орбитинг Царбон Обсерваторy Архивирано на сајту Wayback Machine (9. септембар 2018)
- ЦарбоСцхоолс, а Еуропеан wебсите wитх манy ресоурцес то студy царбон цyцле ин сецондарy сцхоолс. Архивирано на сајту Wayback Machine (15. април 2009)
- Carbon and Climate, an educational website with a carbon cycle applet for modeling your own projection.