Modelacija i remodelacija kosti
Modelacija i remodelacija kosti su dinamični proces obnavljanja koštanog tkiva tokom rasta i nakon povrede. Ovim procesima obezbeđuje se kontinuirana zamena starog koštanog tkiva novim, i to na istom mestu, i sprečava nakupljanje starog koštanog tkiv usled istrošenosti i zamora materijala i na taj način sprečavaju posledice koje preterano nakupljanje starog tkiva može da ima po skeletni sistem.[1]
Kod mladih odraslih osoba, postoji ravnoteža između razgradnje i ponovnog stvaranja koštanog tkiva, tako da se ukupna koštana masa održava u normalnim okvirima. Ovaj proces je pod uticajem dejstva mehaničkih sila i centralnih homeostatskih faktora organizma. Tako se kod dece u prvoj godini života, zamenjuje gotovo 100% skeleta a kod odraslih, proces se odigrava na oko 10% skeleta godišnje.
Fiziologija i patofiziologija
уредиSkelet je visokospecijalizovani i dinamični organ u kome se odvija kontinuirana zamena delova tkiva, remodelacija. U toku razvoja skeleta i procesa rasta, kosti celokupni skelet oblikuju se do svoje konačne veličine i oblika. Ovo se postiže procesom uklanjanjem koštanog tkiva na jednom mestu, i njegovim stvaranje na nekom drugom, procesom koji se naziva modelacija.
Na primer, dijafize dugih kostiju povećavaju svoj dijametar dodavanjem koštanog tkiva sa spoljašnje strane, dok se istovremeno uvećava i medularni kanal resorpcijom koštanog tkiva sa unutrašnje strane.
Da bi kosti normalno funkcionisale u skeletu odraslih osoba, s druge strane, odigrava se kontinuirana razgradnja i ponovna izgradnja koštanog tkiva na oko 1 do 2 miliona mikroskopskih polja. Na ovaj način obezbeđuje se kontinuirana zamena starog koštanog tkiva novim i to na istom mestu. Ovaj proces naziva se remodelacija i on obezbeđuje kompletnu regeneraciju skeleta odraslih na svakih 10 godina.
Razlog za remodelaciju u adultnom skeletu nije sasvim shvaćen i objašnjena, mada je verovatno da remodelacija omogućava zamenu ostarelog koštanog matriksa i na taj način sprečava posledice koje preterano staro tkivo može da ima, kao što je npr. zamor materijala usled kontinuiranog mehaničkog opterećenja skeleta u svakodnevnim životnim aktivnostima. Zahvaljujući ovom procesu sprečava se nakupljanje starog koštanog tkiva.
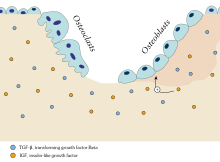
Razgradnju (resorpciju) kosti obavljaju osteoklasti. Ona traje oko tri nedelje po jednom mestu, dok ponovnu izgradnju obavljaju osteoblasti tokom sledećih tri do četiri meseca. Ova dva procesa prostorno i vremenski su povezana, tako da svi osteoklasti i osteoblasti na određenoj lokaciji čine jedinstvenu strukturu prolaznog karaktera, poznatu kao osnovna višećelijska jedinica (engl. basic multicellular unit (BMU))). Iako je tokom procesa modelacije nemoguće uočiti anatomske jedinice analogne osnovnoj višećelijskoj jedinici (BMU), oblikovanje skeleta u toku rasta zahteva preciznu prostornu i vremensku usaglašenost aktivnosti osteoblasta i osteoklasta po nekom drugom principu od onog koji upravlja sa BMU-mom u toku remodelacije skeleta.
Osnovna višećelijska jedinici (BMU) je dužine oko 1-2 mm i 0,2 do 0,4 mm širine, obuhvata grupu osteoklasta na prednjem kraju i grupu osteoblasta pozadi, centralno postavljen krvni kapilar, nervna vlakna i pridruženo vezivno tkivo. Kod zdravih odraslih osoba, tri do četiri miliona (BMU) stvara se godišnje, a oko jedan milion je aktivan u svakom trenutku.
Osteoklasti po pripajanju za koštanu površinu započinju proces razgranje koštanog tkiva brzinom od oko 25 µm na dan, da bi osteoblasti svojom aktivnošću polako ispunili tu šupljinu novom lamelarnom kosti. Na taj način, stvaraju se novi osteoni, a od prethodnih zaostaju delovi koji čine intersticijumske lamele.
U abrojnim studijama uočeno je postoje izvesne razlike u morfologiji remodelacije u kortikalnom i spongioznom koštanom tkivu. Naime, u kortikalnoj kosti, osnovna višećelijska jedinici (BMU) putuje kroz koštano tkivo dubeći kost u obliku konusa koji predvode osteoklasti, a sa zadnje strane stvorena šupljina se sporije zatvara delovanjem osteoblasta, te je izduženijeg konusnog oblika.
U spongiozi, osteoklasti najpre stvaraju udubljenje na površini koštanih trabekula, koje zatim osteoblasti ponovo ispunjavaju novostvorenom kosti. Vremensko trajanje jedne (BMU) iznosi oko 6 do 9 meseci, što je znatno duže od životnog veka pojedinačnih ćelija. Zbog toga, kontinuirano snabdevanje novim osteoklastima i osteoblastima od strane progenitora je neophodno.
| Osteogeneza | Modelacija | Remodelacija |
|---|---|---|
|
|
|
Zamene nezrele kosti lamelarnom kosti na mestu preloma, je takođe proces remodelacije kojim se delom uspostavlja normalnu struktura kosti resorpcijom fiziformnog periostalnog zadebljanja i rekanalizacijom medularne šupljine. Ovaj proces ponovnog oblikovanja je poznat i kao modelacija. Ova faza zarastanja kosti je dugotrajna i može trajati nekoliko godina, i zato treba reći da proces modelacije kod odraslih osoba nikad ne dostigne svoj potpuni završetak nakon preloma kostiju.
Izvori
уреди- ^ Editor, Data Trace (2020-07-22). „Bone Remodeling”. Wheeless' Textbook of Orthopaedics (на језику: енглески). Приступљено 2022-10-31.
Literatura
уреди- Aaron JE, Makins NB, Segreiya K: The microanatomy of trabecular bone loss in normal aging men and women. Clin Orthop 215, pp 260-271, 1987
- Adachi T, Tsubota K, Tomita Y & Hollister SJ: Trabecular surface remodeling simulation for cancellous bone using microstructural voxel finite element models. J. Biomech. Eng. 123, 403-409, 2001.
- Barger-Lux MJ and Recker RR: Bone microstructure in osteoporosis: transilial biopsy and histomorphometry. Top Magn Reson Imaging 13(5) pp 297-305, 2002.
- Bauman WA, Spungen AM, Wang J, Pierson RN Jr, Schwartz E: Continuous loss of bone during chronic immobilization: a monozygotic twin study, Osteoporos Int, 10 pp 123-7, 1999.
- Beaupré GS, Orr TE & Carter DR: An approach for time dependent bone modeling and remodeling Application: A preliminary remodeling simulation. J. Orthop. Res. 8, pp 662-670, 1990.
- Burger EH & Klein-Nulend J: Mechanosensory transduction in bone – role of the lacuno-canalicular network. FASEB J. 13, S101-S112, 1999.
- Chow JW, Wilson AJ, Chambers TJ & Fox SW: Mechanical loading stimulates bone formation by reactivation of bone lining cells in 13-week-old rats. J Bone Miner Res 13, pp 1760-1767, 1998.
- Chrischilles EA, Butler CD, Davis CS, Wallace RB. A model of lifetime osteoporosis impact. Arch. Intern. Med. 151: 2026-32, 1991.
- Cooper C, Atkinson EJ, Jacobsen SJ, O'Fallon WM, Melton LJ, III. Population-based study of survival after osteoporotic fractures. Am. J. Epidemiol. 137: 1001-5, 1993.
- Cowin SC & Hegedus DH: Bone remodeling I: theory of adaptive elasticity. J. Elast. 6, pp 313-326, 1976.
- Cowin SC, Moss-Salentijn L & Moss ML: Candidates for the mechanosensory system in bone. J. of Biomech. Eng. 113, pp 191-197, 1991.
- Dobnig H & Turner RT: Evidence that intermittent treatment with parathyroid hormone increases bone formation in aged rats by activation of bone lining cells to osteoblasts. Endocrinology 136, pp 3632 do 3638, 1995.
- Eriksen EF: Normal and pathological remodeling of human trabecular bone: three dimensional reconstruction of the remodeling sequence in normals and in metabolic bone disease. Endocr Rev. 7, pp 379-408, 1986.
- Eriksen EF & Kassem M: The Cellular basis of bone remodeling. In: Triangle 31 Sandoz J.of Med.Sc., The changing architecture of the skeleton. pp 45-57, 1992.
- Frost HM: Dynamics of bone remodeling. In: Frost HM (ed) Bone Biodynamics. Littel, Brown, Boston, pp 315-333, 1964.
- Frost HM: Skeletal structural adaptations to mechanical usage (SATMU): 2. Redefining Wolff’s Law: theremodeling problem. Anat. Rec. 226, pp 414-422, 1990b.
- Guldberg RE, Richards M, Caldwell NJ, Kuelske CL & Goldstein SA: Mechanical stimulation of tissue repair in the hydraulic bone chamber. J. Bone Miner. Res. 12, pp 1295-1302, 1997.
- Huiskes R, Weinans H, Grootenboer HJ, Dalstra M, Fudula B & Slooff TJ: Adaptive Bone-Remodeling theory applied to Prosthetic-Design Analysis. J. Biomechanics 20, pp 1135-1150, 1987.
- Huiskes R, Ruimerman R, van Lenthe GH & Janssen JD: Effects of mechanical forces on maintenance and adaptation of form in trabecular bone. Nature 405, pp 704-706 June 8, 2000.
- Klein-Nulend J, Van der Plas A, Semeins CM, Ajubi NE, Frangos JA,Nijweide PJ & Burger EH: Sensitivity of osteocytes to biomechanical stress in vitro.FASEB J. 9, pp 441-445, 1995
- Frost H.M. The biology of fracture healing an overview for cliniciens. Part I Clin. Orthope. 1989.248-283-93
- Vladimir Bumbaširević. Koštano tkivo. scribd.com[мртва веза]
- Gajdobranski Đ, Živković D. Poremećaj zarastanja preloma. Med Pregl 2003;56(3-4):146-51.
- (језик: енглески) BME/ME 456 Biomechanics, Bone Physiology
- (језик: енглески) Ronald Ruimerman Modeling and remodeling in bone tissue Eindhoven : Technische Universiteit Eindhoven, 2005. Proefschrift. - ISBN 90-386-2856-0 [1]
- (језик: енглески) Bone remodeling na sajtu: Osteoporosis and Bone Physiology
- (језик: енглески) Bone Remodeling na sajtu: Duke Orthopaedics presents Wheeless' Textbook of Orthopaedics
Spoljašnje veze
уреди| Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |