Membranski receptor
Membranski ili Transmembranski receptori su specijalizovani integralni membranski proteini koji učestvuju u komunikaciji između ćelije i spoljašnjeg sveta. Ekstracelularni signalni molekuli (obično hormoni, neurotransmiteri, citokini, faktori rasta ili ćelijski adhezivni molekuli) se vezuju za receptor, inicirajući promene funkcije ćelije. Ovaj proces se naziva transdukcija signala: Vezivanje inicira hemijsku promenu na intracelularnoj strani membrane. Na taj način receptori igraju jedinstvenu i važnu ulogu u ćelijskog komunikaciji i transdukciji signala.
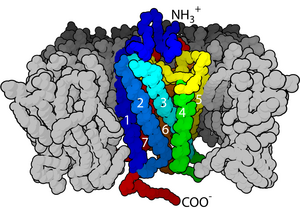
Mnogi transmembranski receptori se sastoje od dve ili više proteinskih podjedinica koje operišu kolektivno i mogu da se disociraju kad se ligandi vežu. Oni su često klasifikovani na osnovu njihove molekulske strukture, ili pošto je detaljna struktura nepoznata za veliku većinu receptora, na osnovu njihove hipotetične (i u pojedinim slučajevima eksperimentalno potvrđene) membranske topologije. Za polipeptidne lance se smatra da premoštavaju lipidni dvosloj samo jednom, dok drugi imaju i po sedam transmembranskih domena (na primer G-protein spregnuti receptori).
Primeri membranskih proteina su glikoproteini i lipoproteini.[1] Stotine membranskih receptora je poznato, a mnogi receptori još nisu otkriveni.[2][3] Skoro svi poznati membranski receptori su transmembranski proteini. Pojedine membrane mogu da imaju nekoliko membranskih receptora sa različitom zastupljenošću na svojoj površini. Pojedini receptori mogu da imaju različite koncentracije na različitim membranskim površinama u zavisnosti od membrane i ćelijske funkcije. Za receptore je uobičajeno da formiraju klastere na površini membrane[4][5], tako da je distribucija receptora na membranskoj površini uglavnom heterogena.
Domeni
уредиP = membrana plazme
I = intracelularni prostor
Kao i svaki drugi integralni membranski protein, transmembranski receptor može da bude segmentiran u tri dela ili domena.
Ekstracelularni domen
уредиEkstracelularni domen je deo receptora izvan membrane na spoljašnjoj strani ćelije ili organele. Ako polipeptidni lanac receptora premoštava dvosloj nekoliko puta, spoljašnji domen se može sastojati od nekoliko "petlji" koje vire izvan membrane. Po definiciji, glavna funkcija receptora je da prepoznaje i proizvodi respons na specifični ligand, na primer neurotransmiter ili hormon (mada pojedini receptori odgovaraju takođe na promene u transmembranskom potencijalu), i u mnogim receptorima ligandi se vezuju za ekstracelularni domen.
Transmembranski domen
уредиKod većine receptora transmembranski alfa heliksi sačinjavaju najveći deo transmembranskog domena. Kod određenih receptora, poput nikotinskog acetilholin receptora, transmembranski domen formira proteinom-okruženu poru kroz membranu, ili jonski kanal. Nakon aktivacije ekstracelularnog domena vezivanjem odgovarajućeg liganda, pora postaje dostupna za jone, koji prolaze kroz nju. Kod drugih receptora, smatra se da transmembranski domeni podležu konformacionoj promeni nakon vezivanja, što uzrokuje intracelularne efekte. Kod nekih receptora, poput članova 7TM superfamilije, transmembranski domen može da sadrži ligand-vezujuće mesto (evidencija za to i za većinu drugih informacija o ovoj klasi receptora je zasnovana delom na studijama bakteriorodopsina i par drugih receptora klase A, čija struktura je bila određena kristalografski).
Intracelularni domen
уредиIntracelularni (ili citoplazmatični) domen receptora interaguje sa unutrašnjošću ćelije ili organele, i prenosi signal. Postoje dva fundamentalno različita načina za ostvarivanje interakcije:
- Intracelularni domen komunicira putem specifičnih protein-protein interakcija sa efektorskim proteinima, koji prenose signal duž signalnog lanca do njegove destinacije.
- Kod enzim-vezanih receptora, intracelularni domen poseduje enzimatsku aktivnost. To je često aktivnost tirozin kinaze. Enzimatska aktivnost može takođe da bude locirana na enzimu vezanom za intracelularni domen.
Vidi još
уредиРеференце
уреди- ^ „MEMBRANE RECEPTORS”. Annual Review of Biochemistry. 43 (0): 169—214. 1974. PMID 4368906. doi:10.1146/annurev.bi.43.070174.001125.
|first1=захтева|last1=у Authors list (помоћ) - ^ Dautzenberg FM, Hauger RL (2002). „The CRF peptide family and their receptors: yet more partners discovered”. Trends Pharmacol. Sci. 23 (2): 71—7. PMID 11830263.
- ^ Rivière S, Challet L, Fluegge D, Spehr M, Rodriguez I (2009). „Formyl peptide receptor-like proteins are a novel family of vomeronasal chemosensors”. Nature. 459 (7246): 574—7. PMID 19387439. doi:10.1038/nature08029.
- ^ Rothberg K.G.; Ying Y.S.; Kamen B.A.; Anderson R.G. (1990). „Cholesterol controls the clustering of the glycophospholipid-anchored membrane receptor for 5-methyltetrahydrofolate”. The Journal of Cell Biology. 111 (6): 2931—2938. PMC 2116385 . PMID 2148564. doi:10.1083/jcb.111.6.2931.
- ^ Côté; Rossi S.G.; Rotundo R.L.; Carbonetto, S. (2001). „The Dystroglycan Complex Is Necessary for Stabilization of Acetylcholine Receptor Clusters at Neuromuscular Junctions and Formation of the Synaptic Basement Membrane”. The Journal of Cell Biology. 152 (3): 435—450. PMC 2195998 . PMID 11157973. doi:10.1083/jcb.152.3.435.
|first1=захтева|last1=у Authors list (помоћ); Пронађени су сувишни параметри:|number=и|issue=(помоћ)
Spoljašnje veze
уреди- IUPHAR GPCR baza podataka Архивирано на сајту Wayback Machine (23. март 2019)
- Cell+Surface+Receptors на US National Library of Medicine Medical Subject Headings (MeSH)