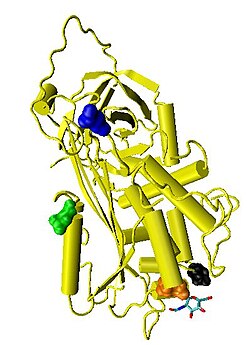
Antitrombin
Antitrombin (AT) je mali proteinski molekul koji inaktivira nekoliko enzima koagulacionog sistem. Antitrombin je glikoprotein koji formira jetra i sastoji se od 432 aminokiselina. On sadrži tri disulfidne veze i četiri moguća mesta glikozilacije. α-Antitrombin je dominantna forma antitrombina nađena u krvnoj plazmi i sadrži oligosaharid u sva četiri mesta glikozilacije. Jedno mesto glikozilacije je konzistentno nezauzeto u drugoj formi antitrombina, β-antitrombinu.[1] Njegova aktivnost se višestruko povećava antikoagulantskim lekom heparinom, koji pojačava vezivanje antitrombina za faktor II i faktor X.
Nomenklatura antitrombina
уредиAntitrombin se takođe naziva antitrombin III (AT III). Oznake antithrombin I do antitrombina IV potiču i ranijih studija tokom 1950-tih.[2]
Antitrombin I (AT I) se odnosi na apsorpciju trombina u fibrin nakon aktivacije trombina fibrinogenom. Antitrombin II (AT II) se odnosi na kofaktor u plazmi, koji zajedno sa heparinom ometa interakciju trombina i fibrinogena. Antitrombin III (AT III) se odnosi na supstancu u plazmi koja inaktivira trombin. Antitrombin IV (AT IV) se odnosi na antitrombin koji postaje aktiviran tokom i kratkotrajno nakon koagulacije krvi.[3] AT III a posebno AT I su medicinski značajni. AT III se generalno odnosi samo na "antitrombin".
Struktura
уредиAntitrombin ima poluživot u krvnoj plazmi od oko jednog dana.[4] Normalna antitrombinska koncentracija u ljudskoj krvnoj plazmi je visoka, oko 0.12 mg/ml, što je ekvivalentno sa molarnom koncentracijom od 2.3 μM.[5]
Antitrombin je izolovan iz plazme velikog broja vrsta.[6] Iz rezultata proteinskog i kDNK sekvenciranja, goveđeg, ovčijeg, zečijeg i mišjeg antitrombina sledi da su oni 433 aminokiseline dugi, što je za jednu aminokiselinu duže od ljudskog antitrombina. Dodatna aminokiselina se javlja u poziciji 6. Antitrombini govečeta, ovce, zeca, moša, i čoveka imaju 84 - 89% identične aminokiseline.[7] Šest aminokiselina formira tri intramolekularna disulfidna mosta, Cys8-Cys128, Cys21-Cys95, i Cys248-Cys430. Svi oni imaju četiri potencijalna mesta N-glikozilacije. Do nje dolazi na asparaginskim (Asn) aminokiselinama sa brojevima 96, 135, 155, i 192 kod ljudi i na sličnim pozicijama kod drugih vrsta. Sva ta mesta su zauzeta kovalentno vezanim oligosaharidnim bočnim lancima u predominantnoj formi ljudskog antitrombina, α-antitrombinu, tako da je molekulska težina ove forme antitrombina 58,200.[1] Potencijalno mesto glikozilacije asparagina 135 nije zauzeto u maje prisutnom obliku (oko 10%) antitrombina, β-antitrombinu.[8]
Rekombinantni antitrombini osobina sličnih normalnom ljudskom antitrombinu su bili proizvedeni koristeći insektne ćelije inficirane bakulovirusom i ćelije sisara gajene u ćelijskoj kulturi.[9][10][11][12] Ti rekombinantni antitrombini generalno imaju različite obrasce glikozilacije u odnosu na normalni antitrombin, i tipično se koriste u strukturnim studijama antitrombina. Mnoštvo antitrombinskih struktura je javno dostupno.
Reference
уреди- ^ а б Bjork, I; Olson, JE (1997). Antithrombin, A bloody important serpin (in Chemistry and Biology of Serpins). Plenum Press. стр. 17—33. ISBN 978-0-306-45698-5.
- ^ Seegers WH, Johnson JF, Fell C (1954). „An antithrombin reaction to prothrombin activation”. Am. J. Physiol. 176 (1): 97—103. PMID 13124503.
- ^ Yin ET, Wessler S. & Stoll PJ. (1971). „Identity of plasma-activated factor X inhibitor with antithrombin 3 and heparin cofactor”. J. Biol. Chem. 246 (11): 3712—3719. PMID 4102937.
- ^ Collen DJ; Schetz F.; et al. (1977). „Metabolism of antithrombin III (heparin cofactor) in man: Effects of venous thrombosis of heparin administration”. Eur. J. Clin. Invest. 7 (1): 27—35. PMID 65284. doi:10.1111/j.1365-2362.1977.tb01566.x.
- ^ Conrad J; Brosstad M.; et al. (1983). „Molar antithrombin concentration in normal human plasma”. Haemostasis. 13 (6): 363—368. PMID 6667903.
- ^ Jordan RE. (1983). „Antithrombin in vertebrate species: Conservation of the heparin-dependent anticoagulant mechanism”. Arch. Biochem. Biophys. 227 (2): 587—595. PMID 6607710. doi:10.1016/0003-9861(83)90488-5.
- ^ Olson ST, Bjork I (1994). „Regulation of thrombin activity by antithrombin and heparin”. Sem. Thromb. Hemost. 20 (4): 373—409. PMID 7899869. doi:10.1055/s-2007-1001928.
- ^ Brennan SO, George PM, Jordan, RE (1987). „Physiological variant of antithrombin-III lacks carbohydrate side-chain at Asn 135”. FEBS Lett. 219 (2): 431—436. PMID 3609301. doi:10.1016/0014-5793(87)80266-1.
- ^ Stephens AW, Siddiqui A. & Hirs CH. (1987). „Expression of functionally active human antithrombin III”. Proc. Natl. Acad. Sci. USA. 84 (11): 3886—3890. PMC 304981 . PMID 3473488. doi:10.1073/pnas.84.11.3886.
- ^ Zettlmeissl G; Conradt HS. (1989). „Characterization of recombinant human antithrombin III synthesized in Chinese hamster ovary cells”. J. Biol. Chem. 264 (35): 21153—21159. PMID 2592368.
- ^ Gillespie LS, Hillesland KK, Knauer DJ (1991). „Expression of biologically active human antithrombin III by recombinant baculovirus in Spodoptera frugiperda cells”. J. Biol. Chem. 266 (6): 3995—4001. PMID 1995647.
- ^ Ersdal-Badju E; Lu A.; et al. (1995). „Elimination of glycosylation heterogeneity affecting heparin affinity of recombinant human antithrombin III by expression of a beta-like variant in baculovirus-infected insect cells”. Biochem. J. 310: 323—330. PMC 1135891 . PMID 7646463.
Literatura
уреди- Panzer-Heinig, Sabine (2009). Antithrombin (III) - Establishing Pediatric Reference Values, Relevance for DIC 1992 versus 2007. Medizinische Fakultät Charité - Universitätsmedizin Berlin.
Spoljašnje veze
уреди- I04.018 MEROPS Архивирано на сајту Wayback Machine (16. октобар 2019)
- Antithrombin+III на US National Library of Medicine Medical Subject Headings (MeSH)